Vezető: Dr. Wiener Zoltán, egyetemi docens
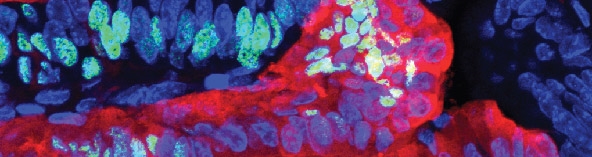

Colorectal cancer (CRC) is one of the leading causes of cancer related death in Hungary and in the Western countries. Despite the progress in understanding colorectal tumorigenesis, this disease still represents an outstanding health problem. Recent reports have proved that not only the tumor cells, but also the stromal cells critically contribute to the tumor progression and patient survival.
The 5-year patient survival is extremely low in pancreatic and lung cancers, partially due to the late diagnosis and the lack of early signs of these diseases.
Our mission is to identify novel communication mechanisms between tumor cells and the stroma that can form the basis of future therapeutic interventions in CRC, PDAC and lung cancer. Furthermore, we aim at identifying novel early biomarkers for lung and pancreatic cancers. One of our interests is the function of the extracellular vesicles that represent a novel form of cell-to-cell communication.

We use a large array of state-of-the-art methods to answer our biological questions, such as the patient-derived organoid technology and the genome editing CRISPR-Cas9 method. Our research group is financed by grants from the Semmelweis University and by the National Research, Development and Innovation Office (Hungary).
2017. november: Kelemen Andrea I. helyezést ért el az ELTE Biológus TDK Konferencián
2018. február: Kovács István III. helyezést ért el a Semmelweis Egyetem TDK Konferenciáján
2018. augusztus: Soós András ÚNKP pályázatot nyert
2018. augusztus: Dr. Zeöld Anikó ÚNKP pályázatot nyert
2018. szeptember: munkacsoportunk telt házas programot készített a Kutatók Éjszakáján
2018. december: Soós András I. helyezett lett az Állatorvosi Egyetem TDK konferenciáján!
2019. február: Kovács István II. helyezést ért el a Semmelweis Egyetem TDK Konferenciáján
2019. április: Soós András I., Kelemen Andrea II. helyezett lett a Biológus Országos TDK-n! Gratulálunk!
2019. április: Wiener Zoltán előadást tartott a Magyar Onkológusok Társasága kecskeméti továbbképző konferenciáján
2019. augusztus: Szvicsek Zsuzsanna ÚNKP pályázatot nyert!
2019. augusztus: Wiener Zoltán meghívott előadóként szerepelt a Magyar Szemlyre Szabott Medicina Társaság gárdonyi konferenciáján
2019. szeptember: munkacsoportunk az idén is nagy érdeklődés mellett szervezett programot a Kutatók Éjszakáján
2019. október: Wiener Zoltán meghívott előadást tartott a Sejtbiológiai Konferencián (Gödöllő)
2019. november: Szvicsek Zuzsanna és Oszvald Ádám megnyerték a Veritas et Virtus Alapítvány díját!
2019. november: Kelemen Andrea megnyerte a Richter Gedeon ösztöndíját!
2019. december: munkacsoportunk nagy érdeklődés mellett programot szervezett a Semmelweis Egészség Napok keretében
2020. június: Wiener Zoltán ismét megnyerte az MTA Bolyai Ösztöndíjat
2020. szeptember: Wiener Zoltán és Soós András ÚNKP pályázatot nyertek!
2020. szeptember: Idan Carmi IV. éves ÁOK TDK hallgató első helyezést ért el a Semmelweis Egyetem TDK Konferencián
2020. december: Sándor Gyöngyvér, Kelemen Andrea és Soós András Semmelweis Tudományos és Innovációs Alap pályázatot nyertek!
2020. december: Wiener Zoltán Semmelweis Tudományos és Innovációs Alap pályázatot nyert
2021. január: Szvicsek Zsuzsanna és Oszvald Ádám summa cum laude minősítéssel megvédték a PhD fokozatukat. Gratulálunk!
2021. február: Idan Carmi IV. éves ÁOK TDK hallgató harmadik helyezést ért el a Semmelweis Egyetem TDK Konferencián
2021. április: Idan Carmi IV. éves ÁOK TDK hallgató megnyerte az OTDK-t!
2021. augusztus: Idan Carmi és Wiener Zoltán ÚNKP pályázatot nyertek!
2021. augusztus: Idan Carmi felvételt nyert az MD-PhD programra
2021. szeptember: Wiener Zoltán megnyerte az OTKA támogatást
2021. szeptember: Idan Carmi megnyerte az OTDK+ konferenciát Szegeden
2021. szeptember: munkacsoportunk ismét önálló programot szervezett a Kutatók Éjszakáján
2021. október: Soós András Nemzet Kiváló Tehetségeiért pályázatot nyert
2021. november: Sándor Gyöngyvér summa cum laude minősítéssel megszerezte a PhD fokozatát. Gratulálunk!
2022. február: valamennyi hallgatónk helyezést ért el a Semmelweis Egyetem TDK Konferenciáján! Seress Iván (I. hely), Idan Carmi (II. hely) és Szabó Dániel Márk (III. hely)
2022. augusztus: Idan Carmi és Wiener Zoltán ÚNKP pályázatot nyertek!
2022. szeptember: Kelemen Andrea summa cum laude minősítéssel megvédte a PhD fokozatát. Gratulálunk!
2023. március: Idan Carmi I. helyezést ért el a Korányi Tudományos Fórumon
2023. május: Soós András utazási ösztöndíjat nyert az European Association for Cancer Research (EACR)-tól
2023. szeptember: Idan Carmi Semmelweis Kiválósági Pályázatot nyert
2023. szeptember: Orosz Adrián felvételt nyert az MD-PhD programba
2023. október: Dr. Hajdó Szabolcs csatlakozott munkacsoportunkhoz
2023. december: Soós András sikeresen megvédte a PhD munkáját
2024. február: Dr. Hajdó Szabolcsot felvették állami ösztöndíjas PhD hallgatónak a Semmelweis Egyetemre

 |
Dr. Wiener Zoltán, egyetemi docens
|
| Dr. Hajdó Szabolcs MD, PhD hallgató |
|
Dr. Idan Carmi MD, PhD hallgató |
|
Dr. Zeöld Anikó, egyetemi adjunktus |
|
|
|
TDK hallgatók |
Kormány Réka, gyógyszerész hallgató Szász Regina, biológus MSc hallgató Maya Litner, MD hallgató Orosz Adrián, MD-PhD hallgató |
| Végzett MSc/MD hallgatók |
Kovács István, MD Szabó Lili, MSc Pápai Márton, MSc Nagy Ádám, MD hallgató Kiss Anna, MD hallgató Szabó Dániel Márk, MD hallgató Seress Iván, MD hallgató |
| Végzett PhD hallgatók |
Oszvald-Haibach Ádám, PhD (2021) Szvicsek Zsuzsanna, PhD (2021) Sándor Gyöngyvér Orsolya, PhD (2022) Kelemen Andrea, PhD (2022) Soós András Áron (2023) |
Oszvald Á, Szvicsek Z, Sándor GO, Kelemen A, Soós AÁ, Pálóczi K, Bursics A, Dede K, Tölgyes T, Buzás EI, Zeöld A, Wiener Z (2019). Extracellular vesicles transmit epithelial growth factor activity in the intestinal stem cell niche. Stem Cells. 2019 Nov 1. doi: 10.1002/stem.3113. IF: 6,022
Szvicsek Z, Oszvald Á, Szabó L, Sándor GO, Kelemen A, Soós AÁ, Pálóczi K, Harsányi L, Tölgyes T, Dede K, Bursics A, Buzás EI, Zeöld A, Wiener Z (2019). Extracellular vesicle release from intestinal organoids is modulated by Apc mutation and other colorectal cancer progression factors. Cell Mol Life Sci. 2019 Apr 26. doi: 10.1007/s00018-019-03052-1. IF: 6,496
Lupsa N, Érsek B, Horváth A, Bencsik A, Lajkó E, Silló P, Oszvald Á, Wiener Z, Reményi P, Mikala G, Masszi T, Buzás EI, Pós Z (2018). Skin-homing CD8+ T cells preferentially express GPI-anchored peptidase inhibitor 16, an inhibitor of cathepsin K. Eur J Immunol. 2018 Dec;48(12):1944-1957. IF: 4,695
Osteikoetxea X, Benke M, Rodriguez M, Pálóczi K, Sódar BW, Szvicsek Z, Szabó-Taylor K, Vukman KV, Kittel Á, Wiener Z, Vékey K, Harsányi L, Szűcs Á, Turiák L, Buzás EI. (2018) Detection and proteomic characterization of extracellular vesicles in human pancreatic juice. Biochem Biophys Res Commun. 2018 Apr 30;499(1):37-43. IF: 2,705
Kivelä R, Salmela I, Nguyen YH, Petrova TV, Koistinen HA, Wiener Z, Alitalo K (2016). The transcription factor Prox1 is essential for satellite cell differentiation and muscle fibre-type regulation. Nat Commun, 7, 13124. IF: 11,329.
Sodar B, Kittel A, Paloczi K, Vukman K, Osteikoetxea X, Szabó-Taylor K, Nemeth A, Sperlágh B, Baranyai T, Giricz Z, Wiener Z, Turiak L, Drahos L, Pallinger E, Vekey K, Ferdinandy P, Falus A, Buzas EI (2016). Low-density lipoprotein mimics blood plasma-derived exosomes and microvesicles during isolation and detection. Sci Rep, in press. IF: 5.578
Együttműködő partnerek:

NVKP_16-0007: Anyagtudományi kutatás és fejlesztés az extracelluláris vezikula alapú orvosdiagnosztika
megvalósításához
A 2017. januárjában indult és 2020. október 31-én lezárult projekt fő célkitűzése volt, hogy az extracelluláris vezikuláknak (EV) egy új, várakozásaink szerint jobb izolálási módszerével megteremtse a lehetőségét az EV-k diagnosztikai felhasználásának. Az ELKH TTK Anyag- és Környezetkémiai Intézet, az USCOM, az Idaco Kft, valamint a Semmelweis Egyetem által alkotott konzorcium keretén belül a Semmelweis Egyetemen elsősorban a pancreas tumorokra, valamint tüdőrákos betegekre fókuszálunk, és a tumorsejtek által kibocsátott EV alpopulációk széleskörű molekuláris jellemzését tűztük ki célul a legmodernebb, high-throughput módszerek és organoidok felhasználásával.
A projektet a Semmelweis Egyetemen belül a Genetikai, Sejt- és Immunbiológiai Intézet és dr. Wiener Zoltán koordinálták, weblapja: https://semmelweis.hu/tcs/kutatocsoportok/nvkp-kutatocsoportok/
A projekt főbb adatai:
Résztvevők:
Pénzügyi adatok:
Futamidő:
Támogató:
Kutatók éjszakája 2021
Ahány sejttípus, annyi tumorféleség. Vajon milyen módszerekkel lehet megismerni az egyes tumorok kialakulásának módját? Hogyan járulnak hozzá a jobb megismeréshez az állatmodellek? Mennyire tekinthetők a genetikailag módosított egerek megfelelőnek, ha az emberi tumorokra vagyunk kíváncsiak? Hogyan tudnánk a betegekből származó rákos szövetet felhasználni a személyre szabott terápiában? Milyen módszerrel lehetne az emberi örökítőanyagot célzottan módosítani? A kötetlen beszélgetésből és gyakorlati részből álló program során két fontos tumortípusra, a vastagbéltumorra és a hasnyálmirigyrákra fókuszálunk. A résztvevőknek lehetőségük nyílik a tudomány mindennapjaiba való belelátásra, egy egyetemi kutatóműhely működésének megismerésére, valamint egy rövid kutatói, laboratóriumi kísérlet elvégzésére is, mellyel személyesen hozzájárulhatnak a tudomány fejlődéséhez....
Mikor? 2021. szeptember 24-én 18 órakor, a program hossza kb. 90 perc.
Hol? Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet, Nagyvárad tér 4, 6-8. emelet. Találkozó az épület portáján.
Szeretettel várunk mindenkit, középiskolás kortól felfelé! Kérjük, hogy védettségi igazolványodat és maszkot hozz magaddal.
A program megvalósult. Találkozunk jövőre!
Kutatók éjszakája 2020
A járványügyi korlátozások miatt 2020-ban munkacsoportunk a programot online, Zoom-on keresztül tartotta meg a Kutatók Éjszakáján, mely interaktív előadásból és beszélgetésből állt.
A nagy érdeklődés mellett megtartott program felvétele elérhető itt:
https://semmelweis.zoom.us/rec/share/bqg8UbFHXXRfZnQJj3Jy7RK3Zv3yp_TYlJ6wY8Rnc1oOGjHf3C1c7lN9eT4u_3BX.ZZy54jtaan_a1GrK
Várunk Titeket 2021-ben is, reméljük, immár személyes formában!
A sokszínű tumorok –kutatói szemmel
Semmelweis Egészség Napok (a program lezajlott)
Ahány sejttípus, annyi tumorféleség. Vajon milyen módszerekkel lehet megismerni az egyes tumorok kialakulásának módját? Hogyan járulnak hozzá a jobb megismeréshez az állatmodellek? Mennyire tekinthetők a genetikailag módosított egerek megfelelőnek, ha az emberi tumorokra vagyunk kíváncsiak? Hogyan tudnánk a betegekből származó rákos szövetet felhasználni a beteg hatóanyagokra való érzékenységének személyes tesztelésére? Milyen módszerrel lehetne az emberi örökítőanyagot célzottan módosítani? A kötetlen beszélgetésből és gyakorlati részből álló program során két fontos tumortípusra, a vastagbéltumorra és a hasnyálmirigyrákra fókuszálunk. A résztvevőknek lehetőségük nyílik a tudomány mindennapjaiba való belelátásra, egy egyetemi kutatóműhely működésének megismerésére, valamint egy rövid kutatói kísérlet személyes elvégzésére is.
Dr. Wiener Zoltán a Semmelweis Egyetemen szerezte doktori fokozatát, jelenleg docensként dolgozik a Genetikai, Sejt- és Immunbiológiai Intézetben. Hat évet töltött posztdoktori kutatóként Helsinki-ben, majd visszatérve megalapította a Molekuláris Onkobiológiai Kutatócsoportot. Aktívan részt vesz a kutatás mellett a magyar, angol és német nyelvű oktatásban is.
Dr. Zeöld Anikó Bécsi Egyetemen szerezte doktori fokozatát, majd az MTA Kísérleti Orvostudományi Kutatóintézet és a Természettudományi Kutatóintézet után 2016-ban csatlakozott a Molekuláris Onkobiológiai Kutatócsoporthoz. Magyar és német nyelven tanít orvostanhallgatókat is.
Az elméleti és gyakorlati részből álló program nyitott mindenki számára (16 éves kortól), aki érdeklődik a tumorok, valamint a kutatás iránt, és szívesen csatlakozik bő egy órára a munkacsoportban folyó kísérletekhez. Előzetes regisztráció szükséges.
Mikor? 2019. december 6-án 18.30 órakor, a hossza kb. 75-80 perc.
Programunk sikeresen megvalósult.